A farmacêutica informou por meio de nota que apresentará os dados do imunizante em “processo de submissão contínua”, por acreditar ser a alternativa “mais célere neste momento”

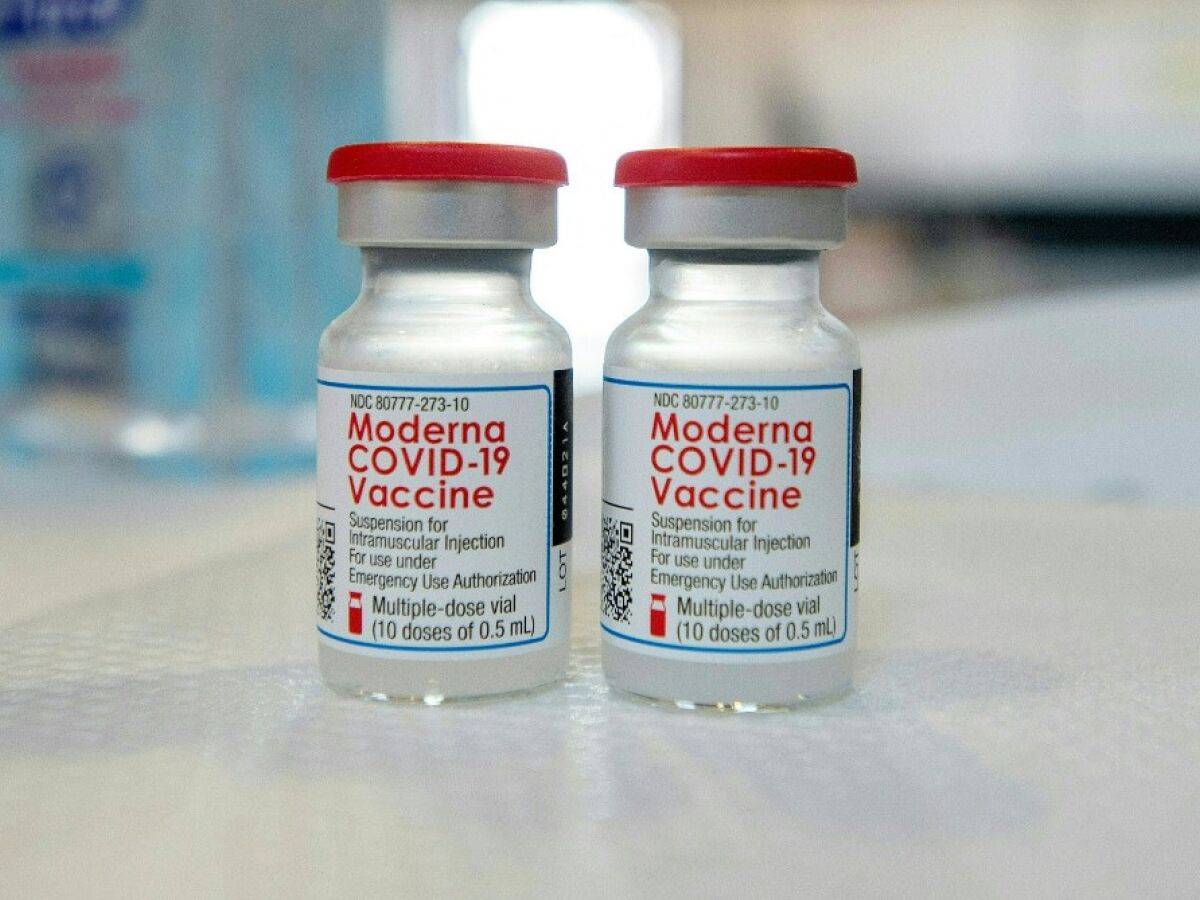
A farmacêutica Pfizer, desenvolvedora de uma vacina contra a Covid-19 ao lado da BioNTech, informou nesta terça-feira (29) que não pedirá à Agência Nacional de Vigilância Sanitária (Anvisa) autorização para uso emergencial do imunizante no Brasil.
Por meio de nota, a Pfizer informou que apresentará os dados da substância em “processo de submissão contínua”, por acreditar ser a alternativa “mais célere neste momento”.
A companhia ainda reclama de uma solicitação da Anvisa para que sejam entregues à agência dados específicos sobre os testes realizados em 3 mil voluntários brasileiros, o que, segundo a Pfizer, “demanda tempo e avaliações estatísticas específicas”.
“Outras agências regulatórias que possuem o processo de uso emergencial analisam os dados dos estudos em sua totalidade, sem pedir um recorte para avaliação de populações específicas”, diz a empresa.
A Pfizer comunicou também que se reuniu com a Anvisa no último dia 14 para esclarecer o processo de submissão da vacina para uso emergencial. Ela afirma ainda que a quantidade de doses de vacina e o cronograma exigidos pela agência podem ser definidos apenas “na celebração do contrato definitivo”. “As condições estabelecidas pela agência requerem análises específicas para o Brasil, o que leva mais tempo de preparação.”
Fonte: Brasil 247